新建制药设施期间典型错误与缺陷
发布日期:2018-08-27
佛山市瑞通认证咨询有限公司(缩写为瑞通认证,http://www.gdruitong.cn/)是一个GMP咨询和执行公司。基于法规要求和我们的实践经验,瑞通认证在此对新建制药设施总结如下内容:
n 为什么讨论新建制药设施?
n 新建制药设施期间典型错误与缺陷
n 新建制药设施的正确项目流程图
n 新建制药设施成功的关键因素
上述内容描述如下:
1. 为什么讨论新建制药设施?
因为:
Ø 如今医药产品的上市时间是关系到企业能否盈利的关键因素。
Ø 竞争对手日益增多,迫使新加入者要有更高的效率。
Ø 越来越复杂的生产工艺,要求相关人员具有更高的能力及对工艺的深入理解。
Ø 愈加严格的法规要求导致更多正式的程序(如确认和验证)。
Ø 客户和官方检查要求制药企业从一开始就有很高的符合性。
Ø GMP厂房的设计和建设需要花费大量的人力、时间和金钱,同时也涉及各种复杂的活动。
Ø GMP厂房的设计和建设应遵循批准的正式的步骤,从而确保相关活动符合GMP法规,并能促使项目快速实施。
2. 新建制药设施期间典型错误与缺陷
新建制药设施期间典型错误与缺陷通常导致违反GMP和注册要求及延误项目。典型错误与缺陷如下所述:
Ø 高层和中层管理人员缺乏质量意识,继而会导致关键缺陷、浪费资源及延误项目,例如没有目标市场,关键设备和设施没有URS,没有施工图纸。
Ø 公司缺乏全面(GMP)项目管理或不完善(缺乏经验)。
Ø 将工程工作视为独立于GMP的活动。
Ø 在开始进行工程项目时,制药企业的质量部门通常没有参与。
Ø 没有根据供应商审计程序进行确认供应商,因此对一些供应商而言,要求他们提供满足工艺和GMP要求的设备及提供必要的文件是困难的(例如焊工的资质,表面抛光度测试报告)。
Ø 确认活动开展得太晚,当设计被发现不正确时,难以变更或为变更需要花费更多的费用,以及项目被延误。
Ø 因为确认活动(如DCS系统)没有在采购过程中进行要求,所以供应商没有充分地参与确认活动。
Ø 文件没有统一的格式,没有文件编码,例如FAT和SAT文件没有采用统一的格式,因此后来不能用于减少确认活动,导致工作量的增加。
Ø 在文件和工厂设计中没有考虑常见缺陷,在建设期间缺失以下活动:
u 异常调查
u 质量工具的应用,例如CAPA、风险评估、变更控制。
u 设备、厂房的设计和维护。
Ø 关键的设备或设施没有URS,那就是说,在DQ、IQ、OQ、PQ时没有参考标准。
Ø 洁净室内设施的设计和建设的技术细节不符合GMP要求,例如在管道安装期间没有考虑斜率,垫圈及润滑油脂的材质证明缺失,没有检查焊接质量。
Ø 确认方案不够详细和合理,例如没有明确定义确认项目的可接受标准,在IQ期间没有检查P&ID图,P&ID图没有更新到最新版本,甚至没有P&ID图。
Ø 质量关键系统和程序应经过验证,但没用风险评估去定义什么是关键的系统和程序,什么可以不需要进行。
3. 新建制药设施正确项目流程图
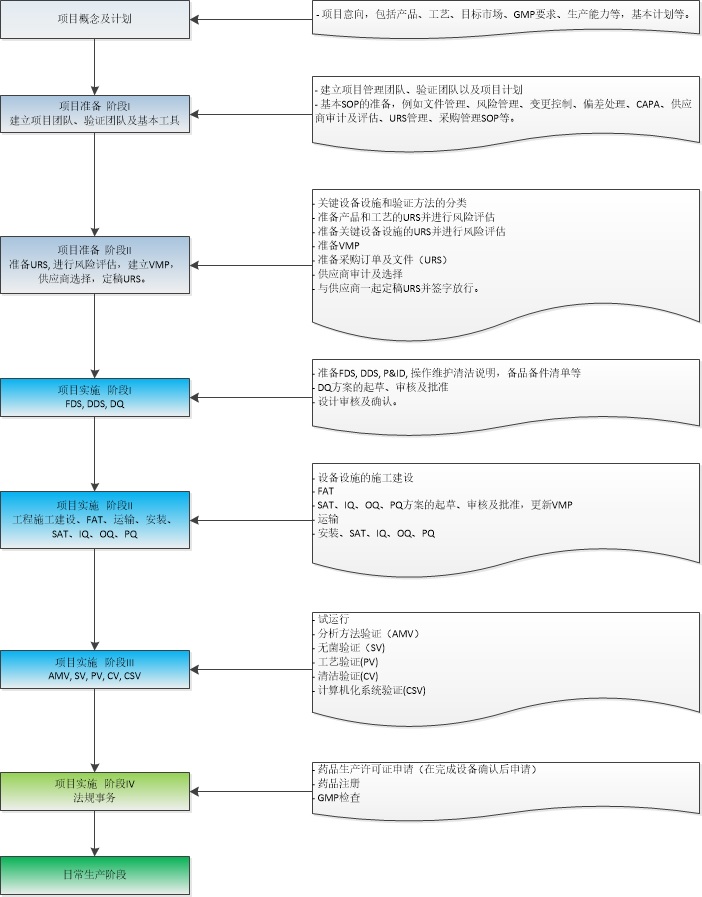
4. 新建制药设施成功的关键因素
Ø 精确地定义包含GMP活动在内的项目计划
Ø 及时建立主文件和程序,例如:
u 文件管理程序
u 培训管理程序
u 验证主计划(VMP)
u 确认和验证程序
u 风险管理程序
u 质量工具:变更控制、偏差处理、CAPA……
u URS管理
u ……
Ø 定义好设计、工程、采购工作流程。
Ø 工艺、关键设备设施的URS的制定, 进行风险评估。
Ø 周密的供应商选择。
Ø 在不同阶段对涉及的员工及供应商提供培训。
佛山市瑞通认证咨询有限公司是 (简称为瑞通认证)是一个GMP咨询和执行公司,位于中国广东省佛山市。主要的服务内容包括GMP咨询和执行、DMF/CEP/ASMF注册及中国药品注册,审计。期待与您真诚的合作。
佛山市瑞通认证咨询有限公司
中国广东省佛山市南海区黄岐广佛1路富威大厦803室
Tel.: +86-136 6005 7841, +86-13695153512
E-mail: ruitong01@gdruitong.cn


